Tin tức
Máy xét nghiệm sinh hóa tự động
TỔNG QUAN về MÁY SINH HÓA TỰ ĐỘNG

① Máy xét nghiệm sinh hóa tự động là gì ?
Máy phân tích hóa sinh, còn được gọi là máy phân tích hóa học lâm sàng, được sử dụng để đo các chất chuyển hóa có trong mẫu sinh học như máu hoặc nước tiểu. Việc nghiên cứu các chất lỏng này giúp chẩn đoán nhiều bệnh. Một ví dụ về việc sử dụng loại máy phân tích này là đo creatinin niệu để đánh giá khả năng lọc của thận.
Máy phân tích hóa học lâm sàng chạy các xét nghiệm trên các mẫu lâm sàng như huyết thanh, huyết tương, nước tiểu và dịch não tủy để phát hiện sự hiện diện của các chất phân tích liên quan đến bệnh tật hoặc thuốc. Máy phân tích hóa học lâm sàng được sử dụng trong nhiều môi trường khác nhau, bao gồm các phòng khám nhỏ, phòng nghiên cứu và phòng thí nghiệm bệnh viện có năng suất cao. Chúng cũng được sử dụng tại điểm chăm sóc, chẳng hạn như trong văn phòng bác sĩ và giường bệnh nhân.
Các chất phân tích thường bao gồm các enzym, chất nền, chất điện giải, protein, thuốc lạm dụng và thuốc điều trị. Kết quả cho các bác sĩ lâm sàng phản hồi về độc tính và chức năng thận, tim và gan.
Khi chọn một máy phân tích sinh hóa tự động, điều quan trọng là phải tính đến việc có cần tự động hóa xét nghiệm hay không, tính đặc hiệu của thuốc thử và mức độ chính xác của phép đo. Cũng cần quan tâm đến dung lượng (số lượng mẫu tối đa được phân tích cùng một lúc).
VIDEO HƯỚNG DẪN SỬ DỤNG QUE THỬ MA TÚY
② Máy phân tích sinh hóa lâm sàng hoạt động như thế nào?
Máy phân tích sinh hóa được tự động hóa cao để tối đa hóa thông lượng, cải thiện sự an toàn của người vận hành khỏi các mối nguy sinh học và giảm nguy cơ lây nhiễm chéo. Các mẫu được nạp vào máy và người dùng lập trình các phép thử. Một đầu dò đo một lượng mẫu và đặt nó vào bình phản ứng. Thuốc thử được thêm vào từ nguồn cung cấp lạnh trên máy. Thời gian ủ được cho phép, nếu được yêu cầu; sau đó đo quang hoặc điện cực chọn lọc ion (ISE) xác định nồng độ của chất phân tích. Kết quả được hiển thị trên màn hình hoặc được gửi đến máy in hoặc máy tính.
③ Máy phân tích hóa sinh sử dụng những loại công nghệ đo lường nào?
Có một số phương pháp đo lường phân tích. Chúng có thể được chia thành hai loại:
?> Kỹ thuật quang học:
Phương pháp đo màu:
Đây là phương pháp phổ biến nhất. Mẫu được trộn với thuốc thử thích hợp để tạo phản ứng tạo màu. Nồng độ của chất phân tích quyết định cường độ của màu thu được.
Phép đo quang:
Một nguồn sáng được chiếu vào mẫu với bước sóng thích hợp trong khi một máy tách sóng quang, đặt ở phía bên kia của mẫu, đo lượng ánh sáng được hấp thụ. Điều này tương quan trực tiếp với nồng độ của chất phân tích trong mẫu. Có một số nguyên tắc ở đây: độ hấp thụ (khả năng của một phương tiện để hấp thụ ánh sáng), turbidimetry (đo lường của mây được tạo ra bởi các chất lơ lửng trong môi trường lỏng), huỳnh quang (ánh sáng phát ra bởi một chất hấp thụ ánh sáng ở một bước sóng và phát ra ánh sáng ở bước sóng khác).

Hình 1 – RX daytona của Randox là một máy phân tích hóa học lâm sàng để bàn nhỏ gọn, hoàn toàn tự động phù hợp để sử dụng trong các phòng thí nghiệm có năng suất vừa và nhỏ.
Nó chạy các phương pháp đo màu và đo quang UV ở tám bước sóng khác nhau từ 340 đến 700 nm, với các tùy chọn điểm cuối, động học, đơn sắc, lưỡng sắc, đo độ đục, mẫu và thuốc thử. Nguồn sáng là đèn vonfram halogen. Một đơn vị ISE tùy chọn có thể được thêm vào. Menu kiểm tra bao gồm hơn 100 bài kiểm tra cho các ứng dụng trong các danh mục sau:
?> Kỹ thuật điện hóa:
Đo điện thế trực tiếp:
Việc sử dụng điện cực chọn lọc ion (ISE) phổ biến và chủ yếu được sử dụng để kiểm tra các ion trong mẫu. Phương pháp này được sử dụng để đo các ion như Na +, K +, CI- và Li +. ISE là cảm biến có khả năng xác định nồng độ của các ion trong dung dịch bằng cách đo dòng điện qua màng chọn lọc ion.
Đo điện thế gián tiếp:
Phương pháp này cũng sử dụng điện cực chọn lọc ion. Nó cho phép thông lượng cao và được sử dụng phổ biến nhất trong các phòng thí nghiệm tập trung. Nó yêu cầu pha loãng trước, không giống như phương pháp đo điện thế trực tiếp và kết quả được biểu thị bằng mol.
Các nhà sản xuất liên tục thêm vào menu thử nghiệm của họ. Ví dụ, Bio-Rad (Hercules, CA; www.bio-rad.com ) gần đây đã giới thiệu Bảng độc tính cho thận Bio-Plex ® Pro ™ RBM mới để định lượng độc tính thận và các dấu hiệu tổn thương thận trong mẫu nước tiểu. Các tấm này tương thích với Đầu đọc đa mặt Bio-Plex MAGPIX ™.
⓸ Phương pháp xử lý mẫu trên máy xét nghiệm sinh hóa tự động
Hầu hết các máy sinh hóa tự động sử dụng phân tích rời rạc, thay vì phân tích dòng liên tục. Trong phân tích rời rạc, các mẫu được tách thành các thùng chứa phản ứng khác nhau, mỗi thùng chứa thuốc thử thích hợp, cho phép thực hiện nhiều phép thử trên cùng một mẫu.
Các loại phương pháp phân tích khác đề cập đến các phương pháp nạp mẫu và sự linh hoạt của lựa chọn xét nghiệm cho từng mẫu và bao gồm phân tích theo lô, ngẫu nhiên, liên tục và STAT. Các phương pháp này được nêu trong Bảng 1 .
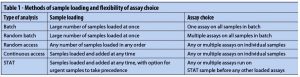
Có ba cách tiếp cận cơ bản với các thiết bị: dòng chảy liên tục, phân tích ly tâm và phân tích rời rạc. Cả ba đều có thể sử dụng phân tích hàng loạt (tức là, số lượng lớn mẫu vật trong một lần chạy), nhưng chỉ những máy phân tích rời rạc mới cung cấp khả năng truy cập ngẫu nhiên hoặc stat.
?> Phương pháp xử lý mẫu dòng chảy liên tục :
chất lỏng (thuốc thử, chất pha loãng và mẫu) được bơm qua một hệ thống ống liên tục. Các mẫu được đưa vào một cách tuần tự, nối tiếp nhau thông qua cùng một mạng. Một loạt bọt khí trong khoảng thời gian đều đặn đóng vai trò là phương tiện phân tách và làm sạch. Do đó, dòng chảy liên tục giải quyết được vấn đề chính về tính đồng nhất trong việc thực hiện các phép thử vì mỗi mẫu đi theo cùng một đường phản ứng. Dòng chảy liên tục cũng hỗ trợ phòng thí nghiệm cần chạy nhiều mẫu yêu cầu cùng một quy trình. Các máy phân tích dòng chảy liên tục phức tạp hơn đã sử dụng các kênh đơn song song để chạy nhiều thử nghiệm trên mỗi mẫu — ví dụ: SMA. Những hạn chế chính đã góp phần vào sự sụp đổ cuối cùng của các máy phân tích dòng liên tục truyền thống (tức là AA và SMA) trên thị trường là những vấn đề đáng kể khi chuyển tải và sử dụng lãng phí thuốc thử liên tục. Câu trả lời của Technicon (nay là Siemens) cho những vấn đề này là mộtmáy phân tích dòng chảy rời rạc (RA1000), sử dụng chất lỏng tiếp cận ngẫu nhiên (chất lỏng hydrofluorocarbon để giảm sức căng bề mặt giữa các mẫu / thuốc thử và ống của chúng) và do đó, giảm hiện tượng chuyển dòng. Sau đó, Chem 1 được phát triển bởi Technicon để sử dụng ống Teflon và dầu Teflon, hầu như loại bỏ các vấn đề chuyển tải. Chem 1 là một máy phân tích dòng liên tục nhưng chỉ có thể so sánh từ xa với nguyên tắc dòng liên tục ban đầu.
?> Phương pháp Phân tích ly tâm :
sử dụng lực tạo ra bởi quá trình ly tâm để truyền và sau đó chứa chất lỏng trong các cuvet riêng biệt để đo ở chu vi của rôto quay . Máy phân tích ly tâm hầu hết có khả năng chạy nhiều mẫu, thử nghiệm một lần, trong một lô. Phân tích hàng loạt là lợi thế chính của chúng vì các phản ứng trong tất cả các cuvet được đọc hầu như đồng thời, không mất nhiều thời gian để chạy một rôto đầy đủ khoảng 30 mẫu so với việc chạy một vài mẫu. Các phòng thí nghiệm có khối lượng công việc cao của các thử nghiệm riêng lẻ để phân tích hàng loạt thông thường có thể sử dụng các thiết bị này. Một lần nữa, mỗi cuvet phải được khớp đồng nhất với nhau để duy trì chất lượng xử lý của từng mẫu. Cobas-Bio (Roche Diagnostics), với đèn flash xenon và cuvet dọc, 6 và IL Monarch, với thiết kế tích hợp hoàn toàn, là hai trong số các máy phân tích ly tâm thành công hơn.
?> Phương pháp Phân tích rời rạc :
là việc tách riêng từng mẫu và các thuốc thử đi kèm trong một vật chứa riêng biệt. Máy phân tích rời có khả năng chạy nhiều phép thử một mẫu tại một thời điểm hoặc nhiều mẫu thử một lần. Chúng là những máy phân tích đa năng và phổ biến nhất và đã gần như thay thế hoàn toàn các máy phân tích ly tâm và dòng chảy liên tục. Tuy nhiên, vì mỗi mẫu nằm trong một bình chứa phản ứng riêng biệt, nên tính đồng nhất về chất lượng phải được duy trì trong mỗi cuvet để chất lượng của một mẫu cụ thể không bị ảnh hưởng bởi không gian cụ thể mà nó chiếm. Các máy phân tích được liệt kê trong Bảng 7.1 là các ví dụ về các máy phân tích rời hiện nay với khả năng truy cập ngẫu nhiên.
⑤ Công suất/ thông lượng máy sinh hóa tự động
Thông lượng được đo bằng số lượng mẫu có thể được kiểm tra mỗi giờ, nhưng tốc độ thay đổi tùy thuộc vào phương pháp kiểm tra. Vì các phép thử so màu có thời gian ủ ngắn nên chúng thường được dành cho các máy có thông lượng cao. Tốc độ thông lượng cho ISE được báo giá riêng. Ví dụ: BioLis 24i của Carolina Liquid Chemistries Corp có thông lượng là 240 trắc quang cộng với 160 mẫu kiểm tra ISE / giờ, dẫn đến tổng thông lượng lên đến 400 mẫu kiểm tra / giờ .
Một phòng thí nghiệm bệnh viện khối lượng lớn có thể yêu cầu thông lượng rất cao. AU5800 được phát triển gần đây từ Beckman Coulter có sức chứa 400 mẫu và thông lượng tối đa 9800 phép thử / giờ và lên đến 1800 phép thử ISE / giờ.
Trong một số cơ sở lâm sàng, tốc độ phân tích quan trọng hơn tốc độ thông lượng cao. PHOx Ultra từ Nova Biomedical thực hiện tới 20 bài kiểm tra chăm sóc quan trọng trong 2 phút. Các tấm thử nghiệm từng phần khác có sẵn trong vòng chưa đầy 1 phút.
⑥ Các bước trong phân tích sinh hóa tự động
Trong hóa học lâm sàng, tự động hóa là cơ khí hóa các bước trong một quy trình. Các quá trình chính do máy phân tích tự động thực hiện có thể được chia thành nhận dạng và chuẩn bị mẫu vật, phản ứng hóa học, thu thập và phân tích dữ liệu. Tổng quan về các quá trình này được cung cấp trong Bảng 7.2 .

Hình 7.2 : Tóm tắt các hoạt động của máy phân tích sinh hóa tự động
Các hoạt động thường diễn ra theo thứ tự được liệt kê từ 1 đến 8. Tuy nhiên, có thể có một số thay đổi nhỏ trong thứ tự. Một số bước có thể bị xóa hoặc trùng lặp. Hầu hết các máy phân tích có khả năng pha loãng mẫu và lặp lại quá trình thử nghiệm nếu nồng độ chất phân tích vượt quá phạm vi tuyến tính của xét nghiệm.
Mỗi bước của phân tích tự động được giải thích trong phần này và một số ứng dụng khác nhau sẽ được thảo luận. Một số thiết bị đã được chọn vì chúng có các thành phần đại diện cho các tính năng phổ biến được sử dụng trong thiết bị đo hóa học hoặc một phương pháp độc đáo để tự động hóa một bước trong quy trình. Không có công cụ đại diện nào được mô tả hoàn toàn, nhưng các thành phần quan trọng được mô tả trong văn bản làm ví dụ.
?> Chuẩn bị và Nhận dạng Mẫu vật
Chuẩn bị mẫu để phân tích đã và vẫn là một quy trình thủ công trong hầu hết các phòng thí nghiệm. Thời gian đông máu (nếu sử dụng huyết thanh), ly tâm và chuyển mẫu vào cốc phân tích (trừ khi sử dụng lấy mẫu ống chính) gây ra sự chậm trễ và tốn kém trong quá trình thử nghiệm. Một giải pháp thay thế cho việc chuẩn bị thủ công là tự động hóa quá trình này bằng cách sử dụng robot, hoặc tự động hóa front-end, để “xử lý” mẫu vật qua các bước này và tải mẫu vào máy phân tích. Một lựa chọn khác là bỏ qua hoàn toàn việc chuẩn bị bệnh phẩm bằng cách sử dụng máu toàn phần để phân tích – ví dụ, Abbott-Vision. Người máy để chuẩn bị bệnh phẩm đã trở thành hiện thực trong một số phòng thí nghiệm lâm sàng ở Hoa Kỳ và các nước khác. Một cách tiếp cận khác là sử dụng ống tách huyết tương và thực hiện lấy mẫu ống chính bằng huyết tương heparin. Điều này giúp loại bỏ sự cần thiết của cả việc đợi mẫu đông lại và lấy mẫu. Thảo luận thêm về xử lý mẫu vật phân tích trước, hoặc tự động hóa giao diện người dùng, sẽ xuất hiện ở phần sau của chương này.
Mẫu phải được xác định đúng cách và vị trí của nó trong máy phân tích phải được theo dõi trong suốt quá trình thử nghiệm. Phương tiện đơn giản nhất để xác định mẫu là đặt cốc đựng mẫu được dán nhãn thủ công vào vị trí phân tích được đánh số trên máy phân tích, phù hợp với bảng tính được chuẩn bị thủ công hoặc danh sách tải do máy tính tạo ra. Cách tiếp cận phức tạp nhất thường được sử dụng ngày nay sử dụng nhãn mã vạch dán vào ống thu gom chính. Nhãn này chứa thông tin nhân khẩu học của bệnh nhân và cũng có thể bao gồm các yêu cầu xét nghiệm.
Sau đó, các ống gắn nhãn mã vạch được chuyển đến vùng tải của máy phân tích, nơi mã vạch được quét và thông tin được lưu trữ trong bộ nhớ của máy tính. Sau đó, máy phân tích có khả năng giám sát tất cả các chức năng nhận dạng, lệnh kiểm tra và thông số, và vị trí mẫu. Một số máy phân tích nhất định có thể nhận các yêu cầu thử nghiệm được tải xuống từ hệ thống thông tin phòng thí nghiệm (LIS) và chạy chúng khi mẫu thích hợp được xác định và sẵn sàng để được dùng pipet.
?> Đo lường và phân phối mẫu vật
Hầu hết các thiết bị sử dụng băng chuyền tròn hoặc giá đỡ hình chữ nhật làm hộp đựng mẫu để giữ cốc đựng mẫu dùng một lần hoặc ống đựng mẫu chính trong khu vực nạp hoặc dùng pipet của máy phân tích. Các cốc hoặc ống này chứa các chất chuẩn, mẫu chứng và mẫu bệnh phẩm được dùng pipet đưa vào các buồng phản ứng của máy phân tích. Các khe trong khay hoặc giá đỡ thường được đánh số để hỗ trợ việc xác định mẫu. Các khay hoặc giá đỡ tự động di chuyển theo các bước ở một vị trí với tốc độ đã chọn trước. Tốc độ xác định số lượng mẫu vật cần phân tích mỗi giờ. Để thuận tiện, thiết bị có thể xác định số rãnh chứa mẫu cuối cùng và kết thúc phân tích sau mẫu đó. Bộ vi xử lý của thiết bị lưu trữ số lượng mẫu trong bộ nhớ và chỉ hút ở các vị trí có chứa mẫu.
Trên máy phân tích VITROS, các khay cốc đựng mẫu là các góc phần tư chứa 10 mẫu mỗi cốc trong các cốc có đáy hình nón. Bốn góc phần tư phù hợp trên một giá đỡ khay ( Hình 7.2 ). Mặc dù khay chứa chỉ chứa được 40 mẫu, nhưng nhiều khay mẫu hơn có thể được lập trình và sau đó được nạp vào vị trí của các khay đã hoàn thành trong khi đang tiến hành thử nghiệm trên các khay khác. Đầu lấy mẫu dùng một lần được nạp bằng tay liền kề với mỗi cốc đựng mẫu trên khay. Máy phân tích Roche / Hitachi có thể sử dụng giá đỡ năm vị trí để giữ mẫu ( Hình 7.3 ). Một máy phân tích mô-đun có thể chứa đến 60 giá đỡ này cùng một lúc.

HÌNH 7.2 VITROS. Bốn khay góc phần tư, mỗi khay chứa mười mẫu, vừa với một giá đỡ khay.

HÌNH 7.3 Giá đỡ năm vị trí Roche / Hitachi
Gần như tất cả các máy phân tích sinh hóa hiện đại đều lấy mẫu từ các ống thu mẫu chính, hoặc đối với các mẫu có thể tích hạn chế, đều có các ống lấy mẫu cực nhỏ. Các ống được đặt trong giá đỡ hoặc băng chuyền. Nhãn mã vạch cho mỗi mẫu, bao gồm tên bệnh nhân và số nhận dạng, có thể được nhà điều hành in theo yêu cầu ( Hình 7.4). Điều này cho phép các mẫu được tải theo bất kỳ thứ tự nào. Máy phân tích thứ nguyên sử dụng một dây đai liên tục gồm các cuvet bằng nhựa dẻo, dùng một lần được đưa qua bể nước của máy phân tích trên đường dẫn động chính. Các cuvet được nạp vào máy phân tích từ một ống chỉ liên tục. Các cuvet này chỉ mục qua thiết bị với tốc độ một lần cứ sau 5 giây và được cắt thành các phần hoặc nhóm theo yêu cầu. Sơ đồ của hệ thống sản xuất và đọc cuvet RxL Kích thước được thể hiện trong Hình 7.5 . Việc để mẫu tiếp xúc với không khí có thể dẫn đến bay hơi mẫu và tạo ra sai sót trong phân tích. Sự bay hơi của mẫu có thể là đáng kể và có thể làm cho nồng độ của các cấu tử được phân tích tăng lên 50% trong 4 giờ. 7Các thiết bị đo chất điện giải, carbon dioxide có trong các mẫu, sẽ bị mất vào khí quyển, dẫn đến giá trị carbon dioxide thấp. Các nhà sản xuất đã nghĩ ra nhiều cơ chế khác nhau để giảm thiểu tác động này — ví dụ, nắp đậy cho khay và nắp riêng lẻ có thể bị xuyên thủng, bao gồm cả việc lấy mẫu ống kín từ ống thu gom chính. số 8
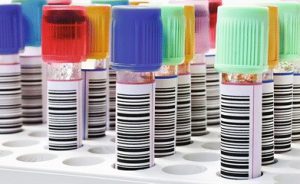
HÌNH 7.4 Các ống thu mẫu được xác định bằng nhãn mã vạch
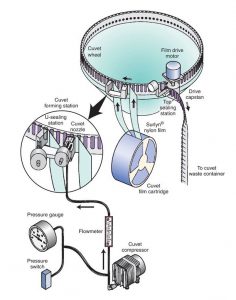
HÌNH 7.5 Hệ thống sản xuất máy phân tích cho các cuvet kín.
Phép đo thực tế của từng phần cho mỗi phép thử phải chính xác. Điều này thường được thực hiện thông qua việc hút mẫu vào một đầu dò . Khi thiết bị rời đang hoạt động, đầu dò sẽ tự động nhúng vào từng cốc mẫu và hút một phần chất lỏng. Sau một khoảng thời gian đặt trước, do máy tính kiểm soát, đầu dò sẽ nhanh chóng nhô lên khỏi cốc. Các đầu dò lấy mẫu trên các dụng cụ sử dụng cốc lấy mẫu cụ thể được lập trình hoặc điều chỉnh để đạt đến độ sâu quy định trong các cốc đó nhằm tối đa hóa việc sử dụng mẫu có sẵn.Những máy phân tích có khả năng hút mẫu từ các ống thu thập chính thường có một đầu dò cảm biến mức chất lỏng song song sẽ kiểm soát sự xâm nhập của đầu dò lấy mẫu đến độ sâu tối thiểu dưới bề mặt của huyết thanh, cho phép hút nhiều phần trong khi tránh làm tắc nghẽn đầu dò với huyết thanh gel tách hoặc cục đông ( Hình 7.6 ).

HÌNH 7.6 Các đầu dò mẫu kép của hệ thống sinh hóa tự động. Lưu ý cảm biến mức chất lỏng ở bên trái của các đầu dò.
Trong máy sinh hóa tự động sử dụng phương pháp dòng liên tục, khi đầu dò mẫu nhô lên khỏi cốc, không khí được hút trong một thời gian xác định để tạo ra bọt khí ở giữa nút mẫu và thuốc thử là chất lỏng. Sau đó, đầu dò đi xuống thùng chứa, nơi dung dịch rửa được hút vào đầu dò và qua hệ thống. Dung dịch rửa thường là nước khử ion, có thể có thêm chất hoạt động bề mặt. Hãy nhớ rằng tất cả các mẫu đều theo cùng một đường phản ứng, sự cần thiết của dung dịch rửa giữa các mẫu trở nên hiển nhiên. Việc nhúng đầu dò vào bể chứa rửa sẽ làm sạch bên ngoài, trong khi hút một lượng nhỏ dung dịch làm sạch lòng mạch. Bể chứa liên tục được bổ sung với lượng dung dịch mới dư thừa. Khoảng thời gian rửa, cộng với bọt khí đã đề cập trước đó, duy trì tính toàn vẹn của mẫu và giảm thiểu việc chuyển mẫu.
Một số loại pipet sử dụng một đầu dùng một lần và một ống tiêm dịch chuyển không khí để đo và cung cấp thuốc thử. Khi điều này được sử dụng, pipet có thể được lập trình lại để đo mẫu và thuốc thử cho các lô thử nghiệm khác nhau một cách tương đối dễ dàng. Bên cạnh việc loại bỏ nỗ lực mồi của hệ thống phân phối thuốc thử bằng dung dịch mới, không có thuốc thử nào bị lãng phí hoặc bị nhiễm bẩn vì không có gì ngoài đầu pipet tiếp xúc với nó.
Việc vệ sinh đầu dò và ống dẫn sau mỗi lần phân phối để giảm thiểu việc chuyển mẫu này sang mẫu tiếp theo là mối quan tâm của nhiều nhà sản xuất. Trong một số hệ thống, thuốc thử hoặc chất pha loãng cũng được phân tán vào cuvet qua cùng một ống và đầu dò. Nước khử ion có thể được phân phối vào cuvet sau khi lấy mẫu để tạo ra độ pha loãng xác định của mẫu và cũng để tráng hệ thống phân phối. Trong Technicon RA1000, chất lỏng truy cập ngẫu nhiên là môi trường tách. Chất lỏng fluorocarbon là một chất nhớt, trơ, không cháy, không bắt lửa, bao phủ hệ thống phân phối. Lớp phủ trên các mặt của hệ thống phân phối ngăn chặn sự truyền tải do làm ướt bề mặt và, tạo thành một nút của dung dịch giữa các mẫu, ngăn cản sự truyền tải do khuếch tán. Một lượng nhỏ (10 μL) chất lỏng này được phân phối vào cuvet cùng với mẫu. Sức căng bề mặt để lại một lớp phủ chất lỏng trong hệ thống phân phối.
Nếu một đầu dò hoặc đầu dò riêng biệt được sử dụng cho từng mẫu và bị loại bỏ sau khi sử dụng, như trong VITROS, thì vấn đề chuyển tiếp là một vấn đề cần bàn. VITROS có một hệ thống phân phối mẫu độc đáo. Một ống hút ấn vào một đầu trên khay mẫu, nhấc nó lên và di chuyển qua mẫu để hút thể tích cần thiết cho các xét nghiệm được lập trình cho mẫu đó. Sau đó, đầu này được chuyển sang khối đo sáng trượt. Khi một trang chiếu ở vị trí để nhận một phần, vòi phun được hạ xuống để giọt 10 μL đã phân phối chạm vào trang chiếu, nơi nó được hấp thụ từ đầu hút. Một piston điều khiển động cơ bước điều khiển sự hình thành hút và thả. Độ chính xác của việc phân phối được quy định ở mức ± 5%.
Trong một số hệ thống rời rạc, đầu dò được gắn bằng một ống không đặt được vào ống tiêm chính xác. Các ống tiêm hút một lượng mẫu xác định vào đầu dò và ống. Sau đó, đầu dò được định vị trên cuvet và mẫu được phân phối. Hitachi 736 sử dụng hai đầu dò mẫu để hút đồng thời một lượng mẫu gấp đôi trong mỗi đầu dò được ngâm trong một hộp chứa mẫu và do đó, phân phối mẫu vào bốn kênh thử nghiệm riêng lẻ, tất cả đều trong một bước vận hành ( Hình 7.7 ). Các đầu dò được nạp sẽ đi qua một bồn tắm phun sương mịn trước khi giao hàng để rửa sạch cặn mẫu bám trên bề mặt ngoài của đầu dò. Sau khi giao hàng, các đầu dò di chuyển đến một trạm rửa để làm sạch bề mặt bên trong và bên ngoài của đầu dò.
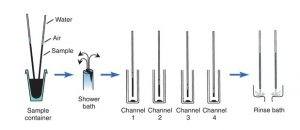
HÌNH 7.7 Hoạt động lấy mẫu của máy phân tích Hitachi 736.
Nhiều máy phân tích hóa học sử dụng động cơ bước được điều khiển bằng máy tính để điều khiển cả ống tiêm lấy mẫu và rửa trôi. Cứ sau vài giây, đầu dò lấy mẫu đi vào hộp chứa mẫu, rút thể tích cần thiết, chuyển đến cuvet và phân phối phần mẫu với một lượng nước để rửa đầu dò. Thể tích rửa trôi được điều chỉnh để mang lại thể tích phản ứng cuối cùng. Nếu vượt quá phạm vi tuyến tính của quy trình, hệ thống sẽ lấy lại ống mẫu ban đầu, lặp lại thử nghiệmsử dụng một phần tư thể tích mẫu ban đầu cho phép thử lặp lại và tính kết quả mới, có tính đến độ pha loãng.
Tính kinh tế của cỡ mẫu là một yếu tố được cân nhắc lớn trong việc phát triển các quy trình tự động, nhưng các phương pháp luận có những hạn chế để duy trì mức độ nhạy và độ đặc hiệu thích hợp. Các yếu tố chi phối phép đo mẫu và thuốc thử phụ thuộc lẫn nhau. Nói chung, nếu kích thước mẫu giảm, thì kích thước của cuvet phản ứng và thể tích phản ứng cuối cùng phải giảm hoặc phải tăng nồng độ thuốc thử để đảm bảo màu sắc phát triển đủ cho các phép đọc trắc quang chính xác.
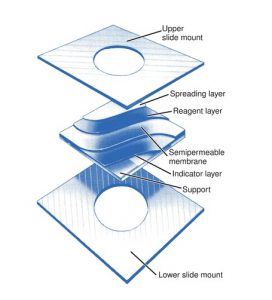
HÌNH 7.8 Trang trình bày VITROS có nhiều lớp chứa toàn bộ hệ thống hóa chất thuốc thử
?> Giai đoạn phản ứng hóa học
Giai đoạn này bao gồm trộn, tách, ủ và thời gian phản ứng. Trong hầu hết các máy phân tích rời rạc, các chất phản ứng hóa học được đựng trong các thùng chứa chuyển động riêng lẻ có thể dùng một lần hoặc tái sử dụng. Các thùng chứa phản ứng này cũng hoạt động như cuvet để phân tích quang học. Nếu các cuvet có thể tái sử dụng, thì các trạm rửa được thiết lập ngay sau các trạm đọc để làm sạch và làm khô các vật chứa này ( Hình 7.9). Sự sắp xếp này cho phép máy phân tích hoạt động liên tục mà không cần thay thế cuvet. Ví dụ về cách tiếp cận này bao gồm máy phân tích ADVIA Centaur (Siemens), ARCHITECT (Abbott Diagnostics), Cobas (Roche Diagnostics) và UniCel DxC Synchron (Beckman Coulter). Ngoài ra, các chất phản ứng có thể được đặt trong một buồng phản ứng tĩnh, trong đó quá trình chảy qua của hỗn hợp phản ứng xảy ra trước và sau khi đọc quang học.

HÌNH 7.9 Các trạm rửa trên máy phân tích sinh hóa tự động thực hiện các công việc sau: (1) hút chất thải phản ứng và phân phối nước, (2) hút và phân phối nước rửa, (3) nước rửa hút và phân phối nước để đo mẫu trắng tế bào, và (4) hút nước tế bào trắng đến khô.
?> Trộn
Một thành phần quan trọng của mỗi quy trình là trộn đều thuốc thử và mẫu. Các nhà sản xuất đã nỗ lực rất nhiều để đảm bảo trộn hoàn chỉnh. Hỗn hợp không đồng nhất có thể gây ra tiếng ồn trong phân tích dòng liên tục và kém chính xác trong phân tích rời rạc.
Quá trình trộn được thực hiện trong các máy phân tích dòng liên tục (ví dụ, Chem 1) thông qua việc sử dụng ống cuộn. Khi dòng thuốc thử và mẫu đi qua các vòng cuộn, chất lỏng sẽ quay và nhào lộn trong mỗi vòng. Tỷ lệ chênh lệch của các chất lỏng rơi qua nhau tạo ra sự trộn lẫn trong cuộn dây.
Hệ thống RA1000 đã tận dụng hành động dừng nhanh của khay phản ứng. Điều này gây ra một hành động va đập vào thành cuvet, nơi trộn các thành phần. Máy phân tích ly tâm có thể sử dụng trình tự bắt đầu – dừng quay hoặc sủi bọt khí qua mẫu và thuốc thử để trộn chúng trong khi các dung dịch này đang chuyển từ đĩa chuyển sang rôto. Quá trình chuyển và trộn này diễn ra chỉ trong vài giây. Lực ly tâm chịu trách nhiệm về sự trộn khi nó đẩy mẫu từ ngăn của nó, qua vách ngăn vào ngăn chứa đầy thuốc thử và cuối cùng là vào không gian cuvet ở chu vi của rôto.
Trong công nghệ VITROS MicroSlide, lớp trải có cấu trúc cho phép mẫu trải đều và nhanh chóng trên (các) lớp thuốc thử để màu phát triển đồng đều.
Hầu hết các máy phân tích hóa học ướt tự động sử dụng cánh khuấy nhúng vào thùng phản ứng trong vài giây để khuấy mẫu và thuốc thử, sau đó chúng trở lại bể chứa rửa ( Hình 7.10 ). Các thiết bị khác sử dụng lực phân phối mạnh mẽ để hoàn thành việc trộn.

HÌNH 7.10 Cánh khuấy trên máy phân tích sinh hóa tự động
? > Phân tách
Trong các phản ứng hóa học, các thành phần không mong muốn gây cản trở quá trình phân tích có thể cần được tách ra khỏi mẫu trước khi đưa các thuốc thử khác vào hệ thống. Protein gây nhiễu lớn trong nhiều phân tích. Một cách tiếp cận mà không cần tách protein là sử dụng tỷ lệ thuốc thử trên mẫu rất cao (mẫu được pha loãng cao) để máy quang phổ không phát hiện được bất kỳ độ đục nào do protein kết tủa gây ra. Một cách tiếp cận khác là rút ngắn thời gian phản ứng để loại bỏ các chất cản trở phản ứng chậm hơn.
Trong các hệ thống dòng chảy liên tục cũ hơn, một bộ lọc là mô-đun tách hoặc lọc. Nó thực hiện tương đương với các quy trình thủ công về kết tủa, ly tâm và lọc, sử dụng màng bóng kính có lỗ mịn. Trong công nghệ VITROS MicroSlide, lớp trải của tấm trượt không chỉ giữ lại các tế bào, tinh thể và các vật chất dạng hạt nhỏ khác mà còn giữ lại các phân tử lớn, chẳng hạn như protein. Về bản chất, những gì đi qua lớp trải là một dịch lọc không có protein.
Hầu hết các máy phân tích rời rạc hiện đại không có phương pháp luận tự động để tách các chất gây nhiễu ra khỏi hỗn hợp phản ứng. Do đó, các phương pháp đã được chọn có ít nhiễu hoặc đã biết các nhiễu mà thiết bị có thể bù đắp được (ví dụ, sử dụng các công thức hiệu chỉnh).
?> Ủ
Bể gia nhiệt trong hệ thống dòng chảy rời rạc hoặc liên tục duy trì nhiệt độ cần thiết của hỗn hợp phản ứng và tạo độ trễ cần thiết để cho phép màu phát triển hoàn toàn. Các thành phần chính của bể sưởi là môi trường truyền nhiệt (tức là nước hoặc không khí), bộ phận làm nóng và bộ điều nhiệt. Nhiệt kế được đặt trong ngăn gia nhiệt của máy phân tích và được theo dõi bởi máy tính của hệ thống. Trên nhiều hệ thống máy phân tích rời rạc, nhiều ống dẫn ủ trong nồi cách thủy được duy trì ở nhiệt độ không đổi thường là 37 ° C.
Công nghệ trượt ủ các phiến kính so màu ở 37 ° C. Có một trạm điều kiện tiên quyết để đưa nhiệt độ của mỗi phiến kính gần 37 ° C trước khi đưa vào tủ ấm. Tủ ấm di chuyển các phiến kính trong khoảng thời gian 12 giây sao cho mỗi phiến kính ở vị trí thoát ra khỏi tủ ấm bốn lần trong thời gian ủ 5 phút. Tính năng này được sử dụng cho các phương pháp tỷ lệ hai điểm và cho phép đọc điểm đầu tiên trong suốt thời gian ủ. Các phiến đo điện thế được giữ ở 25 ° C. Các slide được giữ ở nhiệt độ này trong 3 phút để đảm bảo độ ổn định trước khi đọc.
?> Thời gian phản ứng
Trước khi đọc quang học bằng máy quang phổ, thời gian phản ứng có thể phụ thuộc vào tốc độ vận chuyển qua hệ thống đến trạm “đọc”, bổ sung thuốc thử được hẹn giờ với các buồng phản ứng chuyển động hoặc tĩnh hoặc kết hợp cả hai quá trình. Môi trường có lợi cho việc hoàn thành phản ứng phải được duy trì trong một khoảng thời gian đủ trước khi thực hiện phân tích quang phổ của sản phẩm. Thời gian là một giới hạn nhất định. Để duy trì lợi thế của nhiều lần phân tích nhanh chóng, thiết bị phải tạo ra kết quả càng nhanh càng tốt.
Có thể theo dõi không chỉ sự hoàn thành của một phản ứng mà còn cả tốc độ phản ứng đang tiến hành. Thiết bị có thể trì hoãn phép đo trong một khoảng thời gian xác định trước hoặc có thể đưa ra các hỗn hợp phản ứng để đo trong những khoảng thời gian không đổi. Việc sử dụng các phản ứng tốc độ có thể có hai ưu điểm: tổng thời gian phân tích được rút ngắn và các sắc tố gây nhiễu phản ứng chậm có thể bị phủ nhận. Tốc độ phản ứng được kiểm soát bởi nhiệt độ; do đó, các chức năng của thuốc thử, thời gian và quang phổ phải được phối hợp để hoạt động hài hòa với nhiệt độ đã chọn. Môi trường của cuvet được duy trì ở nhiệt độ không đổi bằng bể chất lỏng, có chứa nước hoặc một số chất lỏng khác có đặc tính truyền nhiệt tốt, trong đó các cuvet chuyển động.
?> Giai đoạn đo lường
Sau khi phản ứng xong, các sản phẩm tạo thành phải được định lượng. Hầu hết tất cả các hệ thống có sẵn để đo đã được sử dụng, chẳng hạn như đo quang tia cực tím, huỳnh quang và ngọn lửa; điện cực cụ thể ion; máy đếm gamma; và máy đo độ sáng. Tuy nhiên, phổ biến nhất là phép đo quang phổ ánh sáng tử ngoại và khả kiến, mặc dù các phương pháp thích ứng của phép đo huỳnh quang truyền thống, chẳng hạn như phân cực huỳnh quang, phát quang hóa học và phát quang sinh học, đã trở nên phổ biến. Ví dụ, Abbott AxSYM là một công cụ phổ biến để phân tích thuốc sử dụng phân cực huỳnh quang để đo các phản ứng xét nghiệm miễn dịch.
Máy phân tích đo ánh sáng yêu cầu một bộ đơn sắc để đạt được bước sóng thành phần mong muốn. Theo truyền thống, các máy phân tích đã sử dụng bộ lọc hoặc bánh xe lọc để tách ánh sáng. Các AA cũ sử dụng các bộ lọc được đặt thủ công vào vị trí trong đường dẫn ánh sáng. Nhiều thiết bị vẫn sử dụng các bánh xe lọc xoay được điều khiển bằng bộ vi xử lý để bộ lọc thích hợp được định vị trong đường đi của ánh sáng. Tuy nhiên, các hệ thống mới hơn và phức tạp hơn cung cấp độ phân giải cao hơn nhờ cách tử nhiễu xạ để phân tách ánh sáng thành các màu thành phần của nó. Nhiều thiết bị hiện nay sử dụng các bộ đơn sắc như vậy với cách tử quay cơ học hoặc cách tử cố định trải các bước sóng thành phần của nó lên một dãy điốt quang cố định — ví dụ, máy phân tích của Hitachi ( Hình 7.11). Sự sắp xếp cách tử sau này, cũng như các bánh xe lọc xoay, dễ dàng đáp ứng phân tích ánh sáng đa sắc, mang lạicải thiện độ nhạy và độ đặc hiệu so với phép đo đơn sắc. Bằng cách ghi lại các số đọc quang học ở các bước sóng khác nhau, máy tính của thiết bị sau đó có thể sử dụng các dữ liệu này để hiệu chỉnh các nhiễu hỗn hợp phản ứng có thể xảy ra ở các bước sóng lân cận cũng như mong muốn.
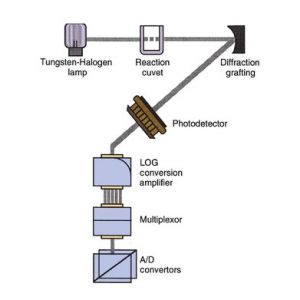
HÌNH 7.11 Máy đo quang dùng cho máy phân tích sinh hóa tự động. Cách tử nhiễu xạ cố định phân tách ánh sáng thành các bước sóng cụ thể và phản xạ chúng vào một mảng cố định gồm 11 bộ tách sóng quang cụ thể. Quang kế không có bộ phận chuyển động.
⑦ Tính năng quản lý dữ liệu trong máy phân tích sinh hóa tự động
Máy thông lượng thấp hiển thị kết quả trên màn hình hoặc có thể có máy in tích hợp. Ưu tiên sẽ là dễ sử dụng và rõ ràng các điều khiển. Máy phân tích EasyRA ® của Medica sử dụng bốn biểu tượng được mã hóa màu để hướng dẫn kỹ thuật viên thông qua tất cả các chức năng của máy phân tích.
Đối với các phòng thí nghiệm lớn, nơi thông lượng có thể lên đến hàng trăm đến hàng nghìn phép thử mỗi giờ, các thiết bị bao gồm phần mềm quản lý dữ liệu và xử lý mã vạch . Thông thường, các máy phân tích có thể được liên kết với LIMS hiện có của bạn .
ADVIA® 1800 , Hệ thống lâm sàng Hóa học từ Siemens trang bị riêng một Windows XP ® máy tính hoạt động với 1 GB RAM và lưu trữ dữ liệu cho 70.000 xét nghiệm bệnh nhân. Các hoạt động bảo trì định kỳ được lập lịch và giám sát bởi phần mềm.
⑧ Chi phí vận hành hệ thống xét nghiệm sinh hóa tự động
Điều quan trọng là phải xem xét chi phí hoạt động cùng với chi phí vốn. Giá thành của thuốc thử và tuổi thọ của thiết bị được đảm bảo khác nhau giữa các nhà sản xuất. Máy đắt hơn có thể tiết kiệm chi phí hơn trong suốt thời gian hoạt động của nó.
Cũng cần xem xét lịch trình bảo trì và thời gian cần thiết để hiệu chuẩn lại, cả về chi phí tài chính và thời gian ngừng hoạt động.
⑨ Tính cơ động của thiết bị
Hầu hết các máy phân tích hóa học lâm sàng được thiết kế để sử dụng trên bàn. Các mô hình nhỏ hơn với menu thử nghiệm hạn chế có sẵn để sử dụng cạnh giường, trong khi các hệ thống thông lượng/ công suất cao toàn diện sẽ yêu cầu không gian sàn.
Máy phân tích đầu giường nhấn mạnh sự nhẹ nhàng, nhỏ gọn và tính di động. Máy Stat pHOx từ Nova Chemical thực hiện các xét nghiệm khí máu cơ bản. Nó có kích thước 12 ”× 12” × 15 ”, nặng dưới 20 lb và vừa với một xe đẩy, nhưng mang đủ thuốc thử cho 7500 phép thử.
Ngược lại, Hệ thống Hóa sinh Tích hợp Dimension ™ RxL Max ™ của Siemens cung cấp đầy đủ hồ sơ trạng thái bệnh với 91 phương pháp (xem Hình 2 ). Nó là một thiết bị đặt trên sàn có kích thước 62,5 ”(159 cm) × 44” (112 cm) × 32 ”(81 cm) và nặng 880 lb
⑩ Khả năng xét nghiệm với mẫu thể tích nhỏ
Bảo tồn máu là quan trọng trong mọi bệnh cảnh lâm sàng, đặc biệt là ở các đơn vị sơ sinh. Làm việc với thể tích siêu nhỏ cũng làm giảm thể tích thuốc thử cần thiết cho mỗi phép thử, giảm chi phí.

Dòng máy phân tích Advia 2400 của Siemens chấp nhận khối lượng mẫu 2-30 ml. Hệ thống sử dụng trung bình 2–3 μL cho mỗi lần thử với thể tích thuốc thử trung bình là 80–120 μL cho mỗi lần thử.
đặt hàng : Hóa chất sinh hóa Beckman Coulter
⑪ Tiêu chí nào được sử dụng để đánh giá hoạt động của máy phân tích hóa sinh?
Một số tiêu chí có thể được sử dụng để đánh giá hiệu suất của thiết bị:
Phương thức hoạt động: Máy phân tích hóa sinh có thể tự động hoặc bán tự động . Trong trường hợp máy phân tích hoàn toàn tự động, mẫu và thuốc thử được chuẩn bị trước và sau đó được đặt vào thiết bị sẽ quản lý và phân tích chúng từ A đến Z. Có thể thiết lập chuỗi thử nghiệm và điều chỉnh tốc độ. Máy phân tích hoàn toàn tự động phù hợp hơn cho các phòng thí nghiệm vừa đến lớn cần phân tích số lượng lớn mẫu.
Mặt khác, các thiết bị bán tự động được thiết kế nhiều hơn cho các phòng thí nghiệm nhỏ hơn hoặc các cơ sở y tế xử lý khối lượng mẫu thấp hơn. Trong những trường hợp này, máy phân tích phải thiết lập từng phép thử riêng lẻ và do đó tốc độ xét nghiệm chậm hơn và không được tự động hóa.
Tỷ lệ: Đây là số lượng mẫu được phân tích mỗi giờ. Tỷ lệ được cải thiện đáng kể với việc sử dụng điện cực chọn lọc ion (xem câu hỏi về các loại công nghệ đo được sử dụng bởi máy phân tích hóa sinh).
Chế độ truy cập ngẫu nhiên: Chế độ này mang lại mức độ linh hoạt cao, đặc biệt cho các phòng thí nghiệm và bệnh viện có mức độ hoạt động từ trung bình đến cao. Họ phải đối mặt với những ràng buộc ngày càng tăng và phải giảm thời gian xử lý trong khi tăng năng suất. Với quyền truy cập ngẫu nhiên, có thể tải mẫu ngẫu nhiên và liên tục và thu được kết quả, từng bệnh nhân, nhanh nhất có thể. Điều này cho phép tỷ lệ đạt được những con số thú vị như 800 bài kiểm tra trắc quang mỗi giờ.
⑫ Thuốc thử và mẫu được quản lý như thế nào?
Điều này sẽ được xác định bởi công suất của máy phân tích. Máy sinh hóa bán tự động chỉ phân tích một mẫu tại một thời điểm. Mặt khác, một thiết bị tự động được chế tạo khác, có hai bể chứa và bao gồm:
Giá để thuốc thử . Chúng thay đổi tùy theo loại mẫu và xét nghiệm được thực hiện.
Một giá để các mẫu cần phân tích được đặt. Chúng thay đổi tùy theo chẩn đoán được thực hiện (chuyên khoa y tế): máu, nước tiểu, dịch não tủy, v.v.
Một cánh tay tự động sẽ hút thuốc thử từ một ống vào ống mẫu với liều lượng mong muốn để phân tích.
Một trong những điểm quan trọng cần xem xét là khối lượng thuốc thử và mẫu mà máy phân tích sẽ cần để thực hiện thử nghiệm. Điều này có thể có tác động đến chi phí hoạt động. Một thiết bị cần lượng lớn thuốc thử sẽ đắt hơn về lâu dài.
Hệ thống có chế độ truy cập ngẫu nhiên (xem câu hỏi về hiệu suất của máy phân tích hóa sinh ) có chế độ quản lý mẫu linh hoạt hơn và tiết kiệm thời gian, đồng thời giảm nguy cơ sai sót của con người do xử lý thủ công. Một ống mã vạch hệ thống cho phép các thiết bị để quản lý các cuộc thử nghiệm đầy đủ, hiệu quả và đáng tin cậy.
⑬ Cân nhắc khi mua máy phân tích hóa học lâm sàng
Khi chọn máy phân tích lâm sàng, hãy nghiên cứu khả năng thông lượng của thiết bị (có thể đạt tới 10.000 ISE kết hợp và thử nghiệm đo màu mỗi giờ), tốc độ thử nghiệm và menu thử nghiệm để chắc chắn rằng nó phù hợp với phòng thí nghiệm của bạn. Chế độ STAT hoặc khả năng truy cập ngẫu nhiên có được yêu cầu không? Phân tích hàng loạt, ngẫu nhiên hay liên tục được ưu tiên? Xem xét nếu phòng thí nghiệm sẽ cung cấp thử nghiệm bổ sung trong tương lai để đảm bảo hệ thống cung cấp các khả năng cần thiết. Hãy nhớ rằng một thiết bị cao cấp hơn sử dụng thuốc thử ít tốn kém hơn có thể tiết kiệm chi phí hơn trong suốt thời gian sử dụng. Các yếu tố bổ sung bao gồm xử lý mẫu, dấu chân của thiết bị và khả năng làm việc với vi điện, một thông số có giá trị trong đơn vị sơ sinh.
Lựa chọn máy phân tích hóa học của bạn sẽ phụ thuộc vào loại xét nghiệm bạn muốn chạy và thông lượng bạn yêu cầu. Các yếu tố khác bao gồm xử lý mẫu, mức độ tự động hóa, quản lý dữ liệu, chi phí vận hành, dấu chân và liệu máy có thể xử lý các mẫu khối lượng nhỏ hay không.
⑭ Tương lai của máy sinh hóa tự động
Những tiến bộ trong máy phân tích hóa học lâm sàng sẽ đồng thời với sự phát triển của các xét nghiệm mới, cải thiện hơn nữa việc chăm sóc bệnh nhân. Các nhà sản xuất đang tùy chỉnh các máy phân tích để sử dụng trong các phòng thí nghiệm nhỏ hơn, sử dụng trong các tình huống có khối lượng rất lớn như trong bệnh viện lớn hoặc tại hiện trường. Khi khả năng phần mềm tiếp tục phát triển, các máy phân tích hóa học lâm sàng sẽ có thể cung cấp tốc độ thử nghiệm và mức độ tự động hóa tăng lên.



